检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
亨廷顿舞蹈症(Huntington’s disease,HD)是一种常染色体显性遗传的神经退行性疾病,此疾病与亨廷顿基因(huntingtin,HTT)1号外显子上CAG三核苷酸的不稳定重复扩增相关。该突变会产生具有毒性的突变亨廷顿蛋白(mutant huntingtin,mHTT),并在神经元中逐渐积累,导致纹状体和大脑皮层神经元退行性损伤。患者通常在中年发病,临床表现为一系列的运动障碍,以躯体舞蹈样运动为典型症状。此外患者还会出现认知功能下降和精神症状。
目前已上市的HD药物均只能暂时缓解症状,治疗效果有限,因此靶向HD的特效药亟待开发。此前研究证明,亨廷顿舞蹈症是由HTT基因突变引起的神经退行性疾病,故由此遗传因素引起的致病过程都可成为潜在的治疗靶标。HD作为单基因显性遗传病,其遗传和致病因素相对简单和明确,因此对 HD 的基因编辑治疗可以作为神经退行性疾病治疗探究的范式。近年来,包括反义寡核苷酸(ASO)、RNA干扰以及CRISPR基因编辑等多种HTT降低策略受到广泛关注。其中,CRISPR/Cas9基因编辑技术能够直接靶向并破坏致病基因,为从源头治疗遗传性疾病提供了新的可能。然而,CRISPR系统在体内长期表达可能带来潜在的脱靶效应和免疫反应等安全风险,也成为其临床应用所面临的重要挑战。
2026年3月18日,PA视讯游戏平台官网李沉简团队在 Science Advances 发表研究成果Self-inactivating AAV-CRISPR at different ages enables sustained amelioration of Huntington’s disease deficits in BAC226Q mice,开发了一种自失活CRISPR基因编辑系统,其在Cas9表达后将破坏自身序列,从而实现Cas9的瞬时表达,同时确保对目标基因的高效编辑。该系统在提高安全性的同时显著改善亨廷顿病小鼠模型的神经病理和行为缺陷,为基因编辑治疗神经退行性疾病提供了新的思路和范式。

论文截图:单载体CRISPR基因编辑系统可显著改善亨廷顿病小鼠表型
李沉简课题组此前成功构建了一种新型的亨廷顿舞蹈症小鼠模型-BAC226Q,该模型携带含有226个CAG重复序列的人源全长HTT基因,能够模拟亨廷顿舞蹈症的病理特征和临床表现(eLife, 2022)。在本研究中,研究团队首先构建了靶向人源HTT基因的SaCas9-sgRNA单载体基因编辑系统,并利用腺相关病毒9(AAV9)将基因编辑工具精准递送至BAC226Q小鼠的大脑纹状体和运动皮层区域。研究人员通过长期的、多时间节点的研究,证明了单次AAV介导的治疗即可实现持续终身的治疗效果。实验结果表明,该CRISPR系统能够高效破坏突变HTT基因,使脑组织中突变亨廷顿蛋白水平降低60%–90%,并显著减少神经元中的异常蛋白聚集。在行为学实验中,接受治疗的小鼠表现出明显改善,包括运动协调能力提升、异常运动行为减少以及体重下降减轻。更令人惊喜的是,该基因编辑治疗还显著延长了亨廷顿病小鼠的寿命。这些结果表明,通过CRISPR基因编辑直接靶向HTT基因,可以从源头上减少致病蛋白,从而显著改善亨廷顿病模型动物的疾病表型。
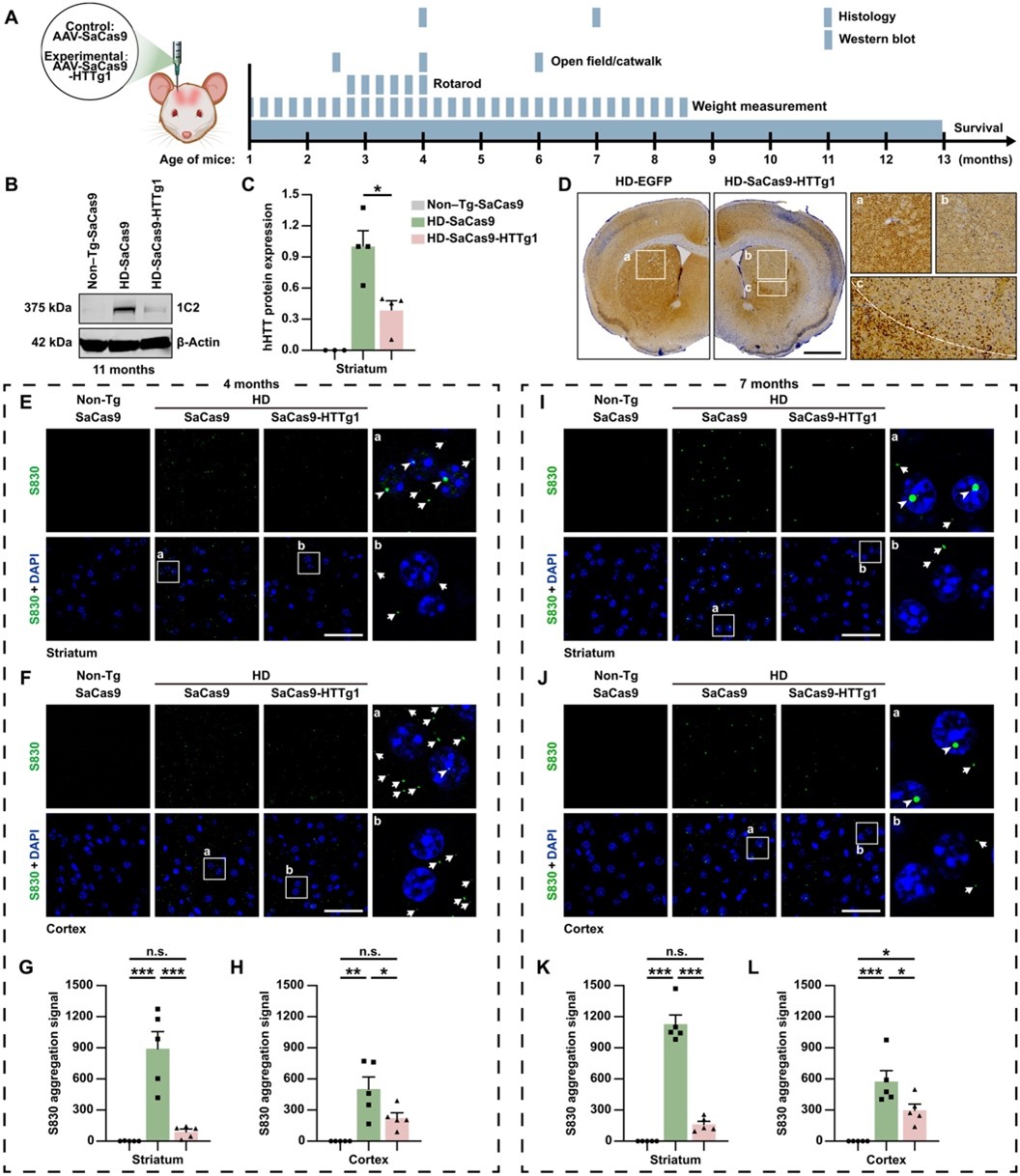
图1. 通过AAV9递送SaCas9-HTTg1进行基因编辑可显著降低BAC226Q小鼠中人源mHTT的水平
不同疾病阶段干预均可产生治疗效果
在临床治疗中,一个重要问题是基因治疗在疾病不同阶段的可能产生的不同干预效果。因此,研究团队进一步系统评估了在不同疾病阶段进行基因编辑的治疗效果。分别在亨廷顿病小鼠模型的三个时间点进行基因编辑干预:疾病发生前阶段、疾病早期阶段以及疾病症状较为严重的晚期阶段。结果发现,在疾病发生前进行干预能够获得最显著的治疗效果,能够有效预防突变蛋白聚集并显著改善行为学表型。值得注意的是,即使在疾病症状已经出现甚至较为严重的阶段进行干预,基因编辑仍然能够显著降低突变蛋白聚集,并延长小鼠存活时间。这一结果表明,即使在疾病进展阶段进行基因治疗,也仍然具有相当程度的潜在治疗价值。
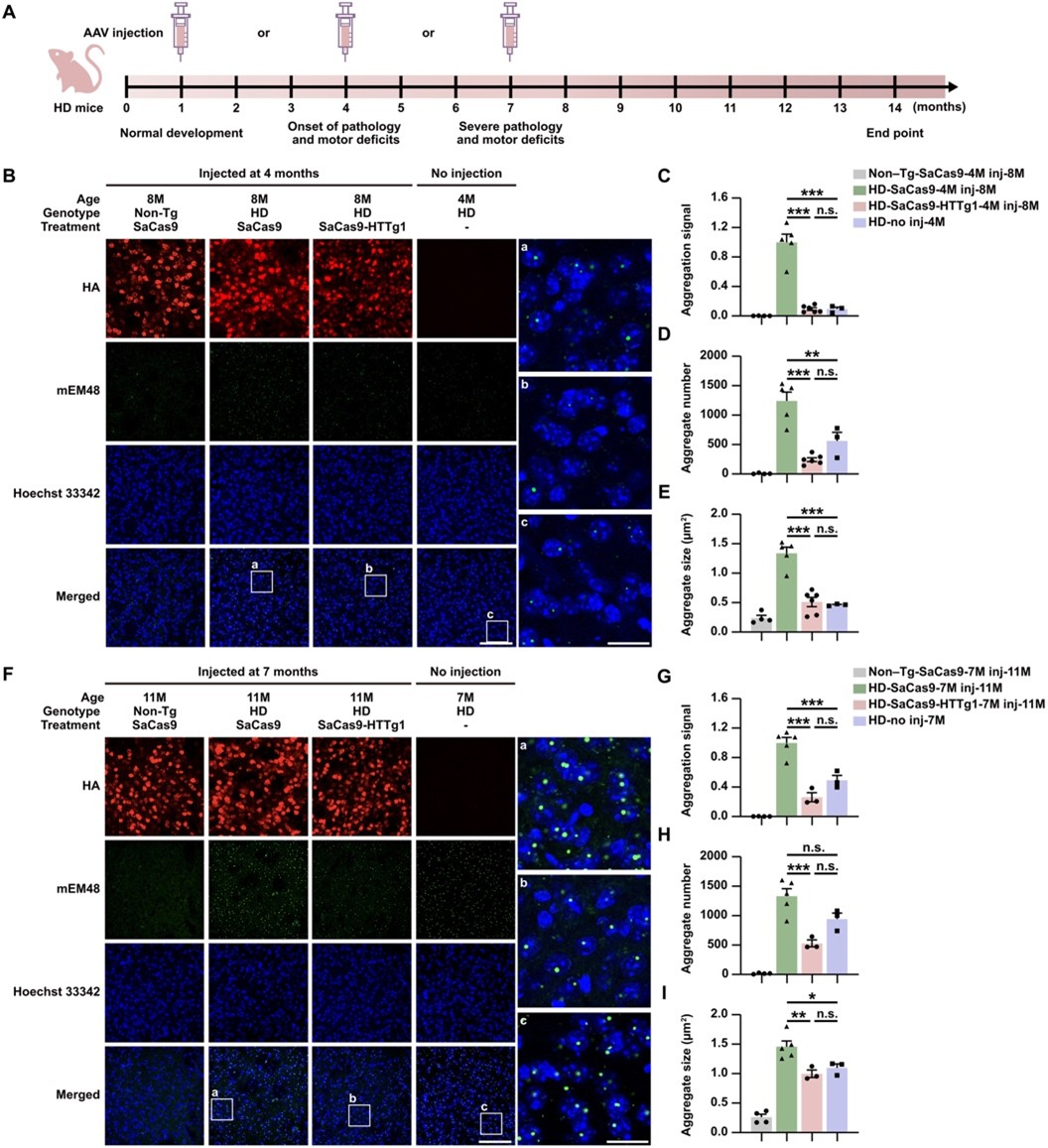
图2. 不同时间点对 BAC226Q 小鼠进行基因编辑干预对抑制 mHTT 聚集的效果存在差异
开发自失活CRISPR系统,提高基因编辑安全性
尽管CRISPR基因编辑具有很大的治疗潜力,但Cas9在体内长期表达可能带来脱靶效应或免疫系统过度激活等安全风险。为解决这一问题,研究团队进一步开发了一种“自失活”(self-inactivating)的CRISPR系统。该系统采用AAV载体,将筛选出的高效编辑HTT基因的sgRNA与SaCas9克隆至同一个载体中;另一个载体则递送筛选出的高效编辑SaCas9的sgRNA。由该双病毒载体构成的自失活系统会在活性蛋白SaCas9表达后破坏Cas9基因,从而缩短核酸酶持续表达的时间。该自失活系统实现了与常规CRISPR/Cas9相当的HTT编辑效率,并将Cas9的表达窗口期限制在一周内。该系统减少了90%的突变亨廷顿蛋白的聚集,并成功地改善了BAC226Q小鼠的运动障碍表型以及延长了小鼠寿命。自失活系统不仅能够降低发生在常规CRISPR/Cas9系统的脱靶事件,并且在人类基因组中尚未出现针对自失活系统的脱靶事件。这一策略在保证治疗效果的同时进一步提高了基因治疗的安全性。
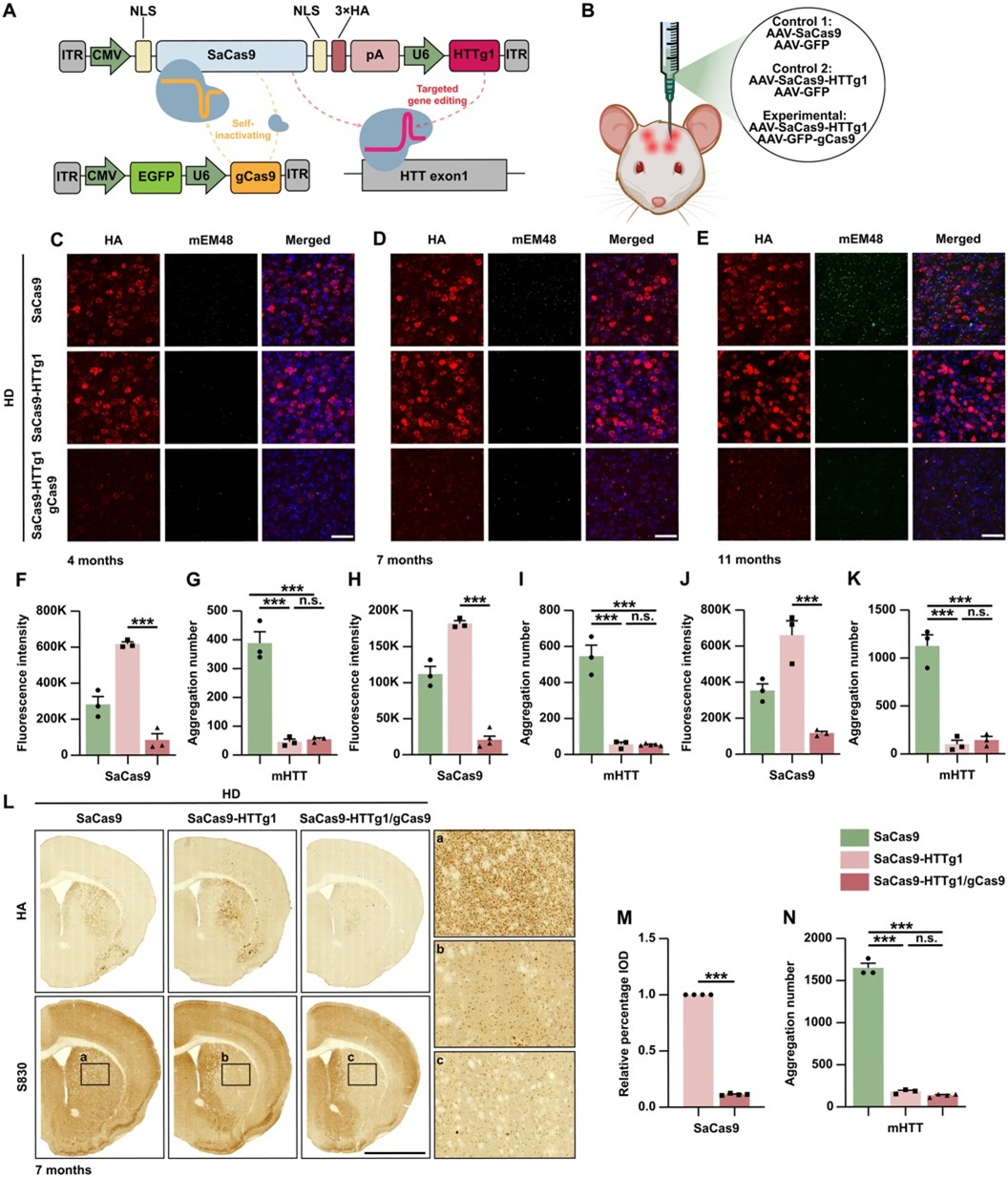
图3. 自失活基因编辑系统在体内可高效降低人源mHTT与Cas9的表达水平
为神经退行性疾病基因治疗提供新策略
该研究表明,通过AAV递送CRISPR基因编辑可以在体内高效且持久地清除突变HTT基因,并显著改善亨廷顿病模型动物的神经病理和行为缺陷。同时,自失活CRISPR系统能够在完成编辑后自动关闭Cas9表达,从而降低潜在的安全风险,为基因编辑治疗神经系统遗传疾病提供了一种更加安全的技术路线。
该研究不仅为利用基因编辑技术治疗亨廷顿病提供了重要的概念验证,也为其他遗传性神经退行性疾病的治疗策略提供了新的思路。未来,研究团队将进一步在灵长类动物模型中评估该系统的安全性和有效性,以推动其向临床应用迈进。
PA视讯游戏平台官网已毕业博士代园祎和祖丽阿耶提·阿卜杜杰力力为论文共同第一作者,李沉简教授和郑素双副研究员为本文共同通讯作者。PA视讯游戏平台官网丁昀奕、黄婉萍、尹健行、欧丽琼及胡家志研究员也为该研究做出了重要贡献。该研究得到了启东创新基金的支持。