检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
内质网相关降解(ER-associated degradation,ERAD)是维持内质网蛋白质稳态的核心质量控制系统。传统观点认为,ERAD的主要功能在于识别、泛素化并清除错误折叠或功能异常的膜蛋白与腔内蛋白。然而,近年来的研究逐渐表明,ERAD不仅承担“纠错”职责,还通过选择性降解部分折叠正确的蛋白,精细调控固醇合成、钙稳态以及内质网与其他细胞器之间的信号传递 (Christianson and Carvalho 2022)。因此,ERAD正被重新定义为一个高度动态的调控平台,而非单纯的蛋白清除通路。
Erlin1/2复合物是定位于内质网膜腔侧的SPFH(Stomatin, Prohibitin, Flotillin, and HflK/C)家族成员。该家族蛋白成员广泛,分布于细胞内不同的膜系统,通常被认为是组织富含饱和脂质的功能性膜微域(Functional membrane microdomain)的支架因子。以往研究表明,Erlin1/2通过调控钙离子通道InsP3R1 (Gao, Bonzerato et al. 2022)以及INSIG、HMG-CoA还原酶等固醇代谢相关蛋白 (Huber, Vesely et al. 2013)的泛素化过程,在钙稳态与膜脂代谢等ERAD相关调控中发挥关键作用。
2026年3月25日,PA视讯游戏平台官网高宁团队、陈晓伟团队与宋晨团队在 Molecular Cell 合作发表题为 “The Erlin1/2 Complex is a Dynamic Scaffold for Membrane Microdomain Assembly on the Endoplasmic Reticulum” 的研究论文。该研究解析了Erlin1/2复合物的冷冻电镜高分辨率结构,并阐明了其在内质网膜上组织膜微域及调控相关蛋白的分子机制。
高宁课题组长期聚焦于SPFH家族蛋白的结构与功能研究,2022年首次报道SPFH家族原核成员HflK/C及其调控的AAA+蛋白酶FtsH复合物的结构,揭示了HflK/C组织膜微域、调节细菌膜蛋白稳态的分子机制 (Ma, Wang et al. 2022)。近年来该课题组致力于真核SPFH蛋白的功能研究,相继报道了Stomatin (Yan, Zhou et al. 2025)、Prohibitin (Luo, Zheng et al. 2025)及Flotillin (Lu, Qian et al. 2026)等成员的分子组装形式及调控机制。在本研究中,团队利用冷冻电镜解析了Erlin1/2复合物的高分辨率结构,探究了其在ER膜蛋白区隔化调控中的重要作用。
研究发现,两个高度同源的Erlin蛋白以交替方式组装成一个由26个亚基构成的穹顶状异源多聚体,从内质网腔侧“倒扣”于膜表面(图1A)。其SPFH1结构域部分嵌入膜中,在腔侧膜叶上划分出一个纳米尺度的圆形膜区域(直径约24 nm),并与该区域共同形成一个近乎封闭的笼状结构。结构数据揭示了Erlin1/2最核心的调控模式——“笼罩(caging)隔离”机制。通过将底物蛋白隔离在微域内部,Erlin1/2能够物理性阻碍其与其他互作蛋白的接触,从而实现功能调控。与此同时,笼体本身又可作为桥联平台,选择性地促进ER膜上特定生物学过程的有序组装与高效运行。
进一步研究显示,单个笼状复合物可在ER膜上划分出纳米尺度的圆形膜微域;多个笼体之间还可能进一步聚集,构建更大尺度的膜功能区。这些区域富集特定脂质,构成内质网的重要功能平台。
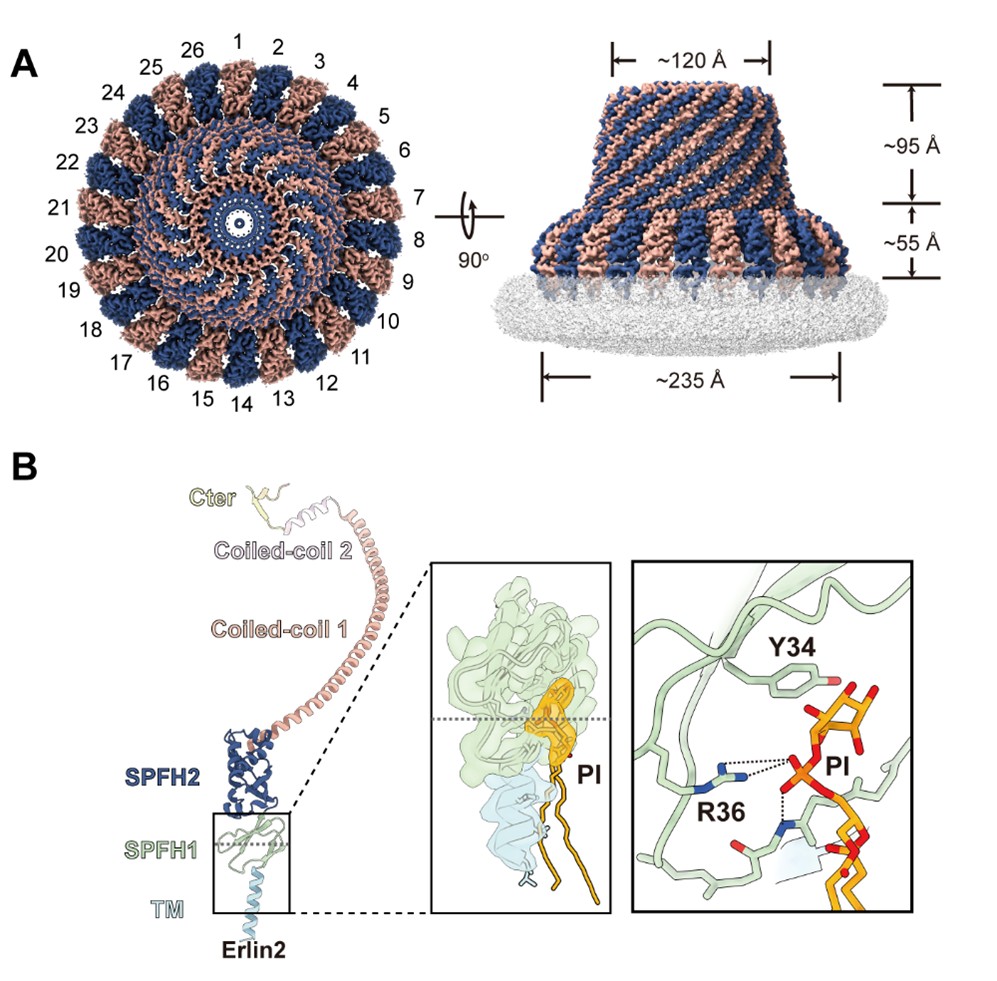
图1. Erlin1/2复合物的冷冻电镜结构
值得注意的是,研究团队在Erlin亚基的插膜结构域中观察到明确的脂质结合密度。通过脂质组学分析,并结合宋晨课题组开展的分子动力学模拟,研究人员确认该脂质为磷脂酰肌醇(phosphatidylinositol,PI)(图1B)。PI及其磷酸化衍生物是细胞信号转导和膜区室特性维持的关键分子。Erlin1/2与PI的结合,可能将PI局部隔离于内质网腔侧膜叶,从而阻止其进一步磷酸化,并可能影响下游信号分子的生成与功能。这一发现为理解Erlin复合物如何调控膜脂代谢提供了重要线索。
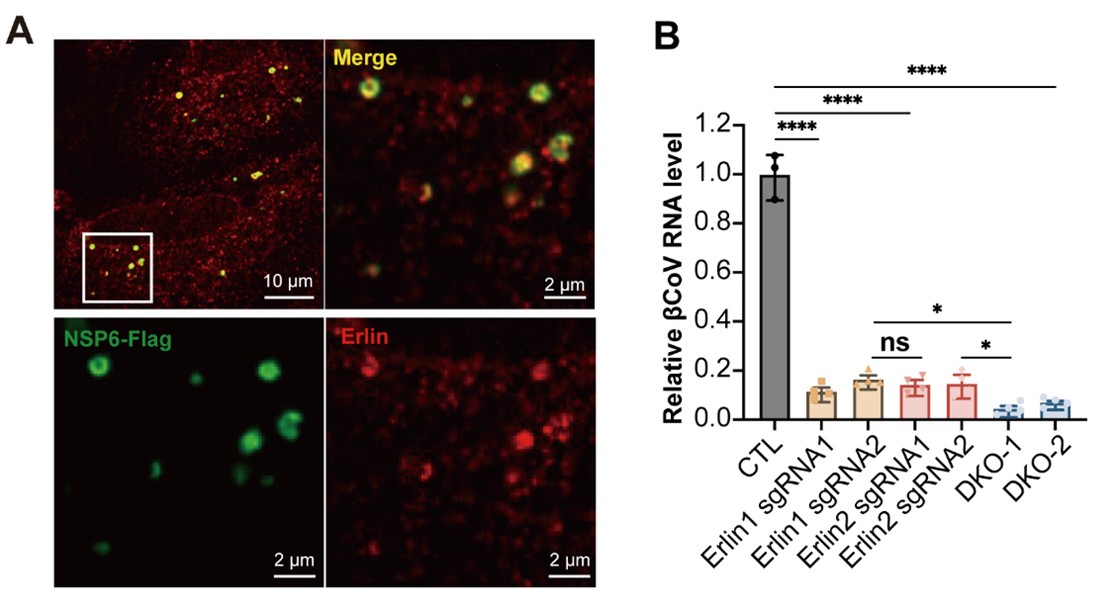
图2. Erlin1/2复合物参与冠状病毒的RNA复制
陈晓伟团队长期从事脂质代谢研究,聚焦内质网脂层平衡在维系细胞与机体稳态中的基础性作用,并借助病毒对宿主脂质代谢的胁持作为工具开展研究。研究团队通过鼠源冠状病毒感染实验发现,Erlin复合物可被病毒蛋白NSP6招募,并参与冠状病毒RNA复制过程(图2)。值得关注的是,近期国际团队研究还报道Erlin在病毒包装成熟阶段可能发挥抑制作用,可能与其调控胆固醇代谢相关 (Teo, Wong et al. 2023)。这提示Erlin在病毒感染过程中具有阶段依赖性的双重调控功能。
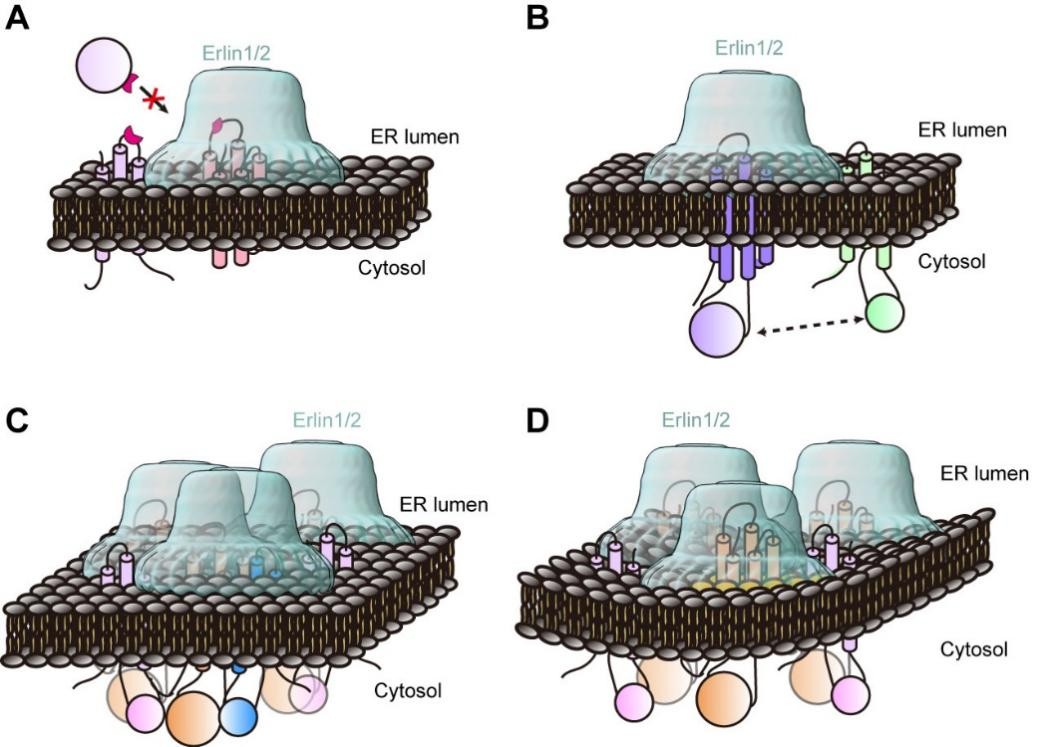
图3. Erlin1/2复合物介导膜微功能域组织及蛋白调控的机制模型
总体而言,本研究从结构层面揭示了Erlin1/2如何通过构建笼状多聚体,在内质网膜上组织功能性膜微域,并通过空间隔离与桥联机制调控蛋白功能(图3)。这一发现不仅为理解ERAD调控机制提供了重要结构框架,也为阐明膜微域组织与细胞功能之间的联系奠定了基础。
PA视讯游戏平台官网闫璐博士、前沿交叉学科研究院22级博士生徐子弘、未来技术学院22级博士生姚远航以及定量生物学中心Tadsanee Awang博士为论文共同第一作者;PA视讯游戏平台官网高宁教授、陈晓伟教授以及宋晨教授为共同通讯作者。本研究同时得到了北大-清华生命联合中心、核糖核酸北京研究中心、PA视讯游戏平台官网冷冻电镜平台、PA视讯游戏平台官网电镜平台及成像平台、膜生物学全国重点实验室以及清华大学脂质质谱平台的支持。
原文链接:https://www.cell.com/molecular-cell/fulltext/S1097-2765(26)00157-7
参考文献:
1. Christianson, J. C. and P. Carvalho (2022). "Order through destruction: how ER-associated protein degradation contributes to organelle homeostasis." Embo j 41(6): e109845.
2. Gao, X., C. G. Bonzerato and R. J. H. Wojcikiewicz (2022). "Binding of the erlin1/2 complex to the third intralumenal loop of IP(3)R1 triggers its ubiquitin-proteasomal degradation." J Biol Chem 298(6): 102026.
3. Huber, M. D., P. W. Vesely, K. Datta and L. Gerace (2013). "Erlins restrict SREBP activation in the ER and regulate cellular cholesterol homeostasis." J Cell Biol 203(3): 427-436.
4. Lu, M.-A., Y. Qian, L. Ma, J. Hong, X. Li, L. Yu, Q. Guo and N. Gao (2026). "Molecular mechanisms of flotillin complexes in organizing membrane microdomains." Nature Communications.
5. Luo, D., L. Zheng, M.-A. Lu, Z. Chen, P. Wang, Q. Guo and N. Gao (2025). "Structural basis for prohibitin-mediated regulation of mitochondrial m-AAA protease." bioRxiv: 2025.2004.2015.648916.
6. Ma, C. Y., C. K. Wang, D. Y. Luo, L. Yan, W. X. Yang, N. N. Li and N. Gao (2022). "Structural insights into the membrane microdomain organization by SPFH family proteins." Cell Research 32(2): 176-189.
7. Teo, Q. W., H. H. Wong, T. Heunis, V. Stancheva, A. Hachim, H. Lv, L. Siu, J. Ho, Y. Lan, C. K. P. Mok, R. Ulferts and S. Sanyal (2023). "Usp25-Erlin1/2 activity limits cholesterol flux to restrict virus infection." Dev Cell 58(22): 2495-2509.e2496.
8. Yan, L., X. Zhou, M. Li, C. Wang, B. Xiao, P. Xi, P. Zou and N. Gao (2025). "Structural Role of Stomatin in Organizing Functional Membrane Microdomains." bioRxiv: 2025.2008.2030.673307.